علم الكيمياء

تاريخ الكيمياء والعلماء المشاهير

التحاضير والتجارب الكيميائية

المخاطر والوقاية في الكيمياء

اخرى

مقالات متنوعة في علم الكيمياء

كيمياء عامة


الكيمياء التحليلية

مواضيع عامة في الكيمياء التحليلية

التحليل النوعي والكمي

التحليل الآلي (الطيفي)

طرق الفصل والتنقية


الكيمياء الحياتية

مواضيع عامة في الكيمياء الحياتية

الكاربوهيدرات

الاحماض الامينية والبروتينات

الانزيمات

الدهون

الاحماض النووية

الفيتامينات والمرافقات الانزيمية

الهرمونات


الكيمياء العضوية

مواضيع عامة في الكيمياء العضوية

الهايدروكاربونات

المركبات الوسطية وميكانيكيات التفاعلات العضوية

التشخيص العضوي

تجارب وتفاعلات في الكيمياء العضوية


الكيمياء الفيزيائية

مواضيع عامة في الكيمياء الفيزيائية

الكيمياء الحرارية

حركية التفاعلات الكيميائية

الكيمياء الكهربائية


الكيمياء اللاعضوية

مواضيع عامة في الكيمياء اللاعضوية

الجدول الدوري وخواص العناصر

نظريات التآصر الكيميائي

كيمياء العناصر الانتقالية ومركباتها المعقدة


مواضيع اخرى في الكيمياء

كيمياء النانو

الكيمياء السريرية

الكيمياء الطبية والدوائية

كيمياء الاغذية والنواتج الطبيعية

الكيمياء الجنائية


الكيمياء الصناعية

البترو كيمياويات

الكيمياء الخضراء

كيمياء البيئة

كيمياء البوليمرات

مواضيع عامة في الكيمياء الصناعية

الكيمياء الاشعاعية والنووية
معادلات الحالة لغاز حقيقي
المؤلف:
د. نضال الرشيدات
المصدر:
دِيناميكا حَراريَّة
الجزء والصفحة:
ج2 ص6
1-1-2016
3881
معادلة فان درْ فالس The Van der Waals equation
هناك نوعان من معادلات الحالة التي اقترحت لتفسير سطوح P-v-T للغازات الحقيقية:
- تلك المبنيَّة على التجربة (empirical) والتي تستنج معاملاتها منها،
- وتلك المُستمدَّة من نظريَّة الغاز أو النظريَّة الحركيَّة kinetic theory.
يشترك النوعان في خاصيَّة مهمة جداً وهي أنَّ هذه المعادلات يجبُ أنْ تؤول إلى معادلة الحالة لغاز حقيقي عند حجوم نوعيَّة كبيرة نسبياً. من بيْن هذه المعادلات تتمَّيز معادلة فان درْ فالس التالية من حيثُ بساطتها وفي نفس الوقت قدرتُها على تفسير ظواهر كثيرةٍ خاصة بالغازات.
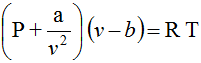
حيثُ a و b ثابتان لغازٍ ما. تختلف قيمة الثابتيْن من غاز لآخر وفي الجدول 1-2 التالي قيمة a و b لبعض الغازات.
|
المادة |
a (J m3 kilomole-2) |
b (m3 kilomole-1) |
|
الهيليوم He |
3.44 ´ 103 |
0.0234 |
|
الهيدروجين H2 |
24.8 |
0.0266 |
|
الأكسجين O2 |
138 |
0.0318 |
|
ثاني أُكسيد الكربون CO2 |
366 |
0.0429 |
|
الماء H2O |
580 |
0.0319 |
|
الزئبق Hg |
292 |
0.0055 |
الجدول 1-2: قيم ثابتي فان درْ فالس a و b
 الاكثر قراءة في مواضيع عامة في الكيمياء الفيزيائية
الاكثر قراءة في مواضيع عامة في الكيمياء الفيزيائية
 اخر الاخبار
اخر الاخبار
اخبار العتبة العباسية المقدسة

الآخبار الصحية















 قسم الشؤون الفكرية يصدر كتاباً يوثق تاريخ السدانة في العتبة العباسية المقدسة
قسم الشؤون الفكرية يصدر كتاباً يوثق تاريخ السدانة في العتبة العباسية المقدسة "المهمة".. إصدار قصصي يوثّق القصص الفائزة في مسابقة فتوى الدفاع المقدسة للقصة القصيرة
"المهمة".. إصدار قصصي يوثّق القصص الفائزة في مسابقة فتوى الدفاع المقدسة للقصة القصيرة (نوافذ).. إصدار أدبي يوثق القصص الفائزة في مسابقة الإمام العسكري (عليه السلام)
(نوافذ).. إصدار أدبي يوثق القصص الفائزة في مسابقة الإمام العسكري (عليه السلام)