


 علم الكيمياء
علم الكيمياء 
 الكيمياء التحليلية
الكيمياء التحليلية 
 الكيمياء الحياتية
الكيمياء الحياتية 
 الكيمياء العضوية
الكيمياء العضوية 
 الكيمياء الفيزيائية
الكيمياء الفيزيائية
 الكيمياء اللاعضوية
الكيمياء اللاعضوية 
 مواضيع اخرى في الكيمياء
مواضيع اخرى في الكيمياء
 الكيمياء الصناعية
الكيمياء الصناعية |
أقرأ أيضاً
التاريخ: 28-5-2021
التاريخ: 18-5-2021
التاريخ: 16-12-2019
التاريخ: 17-10-2021
|
طبيعة الأحماض الامينية :
ان انتظام المجاميع الأربعة في الاحماض الامينية حول ذرة الكربون (ألفا) تكسب الحامض الأميني نشاطاً ضوئياً، فجميع الأحماض الامينية العشرون عدا حامض الكلايسين (Gly) تعطي انداداً بصرية بسبب امتلاكها ذرة كربون غير متناسقة (كيرالية) لذلك فان هذه الاحماض توجد في الطبيعة على شكلين، الشكل الأول يسمى L- أيزومير (L – isomer) والثاني يسمى – D - أيزومير (D- isomer).
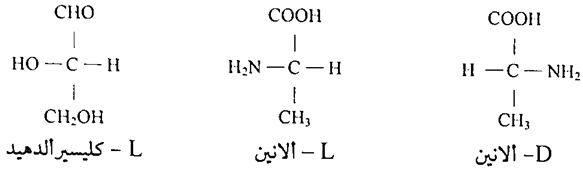

وتتكون عادة كل البروتينات في جسم الإنسان من الاحماض الامينية شكل (L). ان العشرين حامض أميني الداخلة في تركيب البروتينات تمتلك سلاسلا جانبية مختلفة في الشكل والحجم والشحنة والتركيب الكيميائي. ان البروتينات في جميع الاجناس من البكتريا حتى الإنسان تتألف من نفس مجموعة العشرون حامض أميني.
ان الاساسيات الأبجدية للجزيئات البروتينية يرجع عمرها الى ما لا يقل عن بليون سنة. وهذا الطيف من التنوع في الوظائف التي تؤديها الجزيئات البروتينية ناتج عن الاختلاف والتنوع في استثمار العشرين نوعاً من الاحماض الامينية في تشكيل الجزيئات البروتينية.
وسوف نلقي نظرة موجزة عن هذه الاحماض الامينية من حيث الطبيعة الكيميائية والمجاميع الجانبية وبيان مدى تأثيرها على الصفات الكيميائية والفيزيائية لهذه الاحماض والتي تعتبر الوحدات الأساسية في تشكيل كافة الجزيئات البروتينية المعروفة :

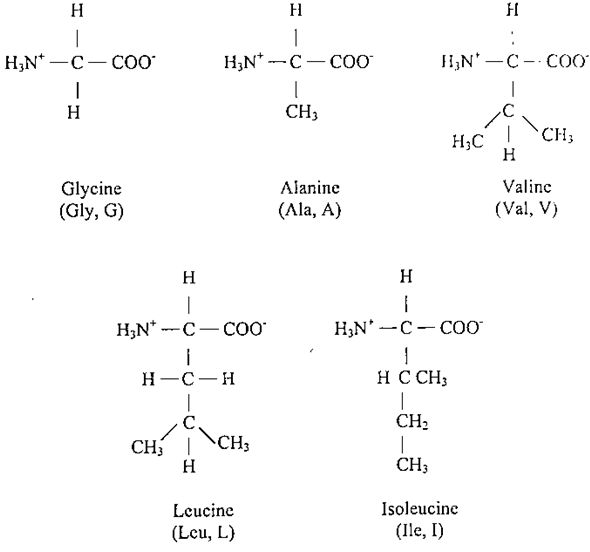
ان اختلاف السلاسل الجانبية الهيدروكاربونية في الجسم والشكل يمكنها من التراص معاً لتكوين مركبات محبوكة التركيب يتخللها قليل من المساحات البينية الصغيرة.
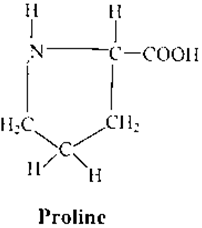
ان حامض البرولين (Pro , P) هو الآخر يحتوي على سلاسل جانبية اليفانية ولكنها تختلف عن باقي أعضاء المجموعة العشرين في كون سلسلته الجانبية مرتبطة بكل من ذرة النتروجين للمجموعة الأمينية وذرة الكربون (ألفا)، والمركب الحلقي الناتج يؤثر في الشكل البنائي الهندسي للجزيئات البروتينية. وغالبا ما نرى البرولين موجودا عند الالتواء في الجزيئات البروتينية المطوية وهو غير كاره للماء، ويلاحظ كذلك ان البرولين (Proline) يحتوي على مجموعة أمينية ثنائية الارتباط وليست أولية الارتباط، مما يجعله حامضا أمينياً من نوع (lmino Acid).


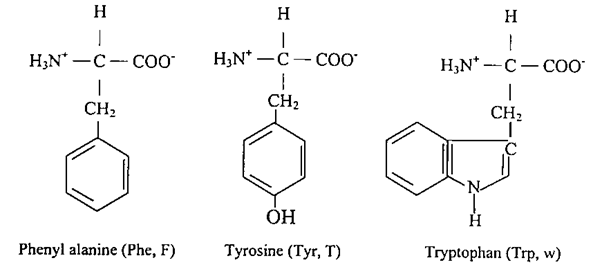
ان الاحماض الامينية التي تم التطرق إليها حتى الان تحتوي على الحلقة الأروماتية مثل الفنيل آلانين والتربتوفان والتايروسين التي لها القدرة على سحب الإلكترون (باي Pi – electron-) العديمة التوضع يجعلها قادرة على التفاعل مع النظم – باي (Pi – System) الأخرى وتستطيع نقل الإلكترونات.

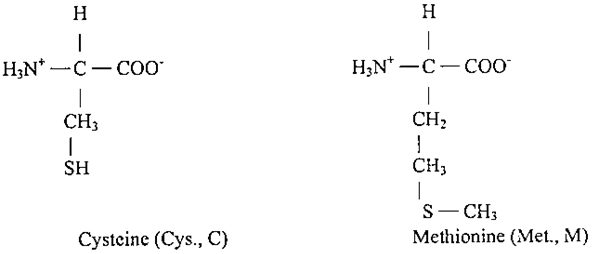
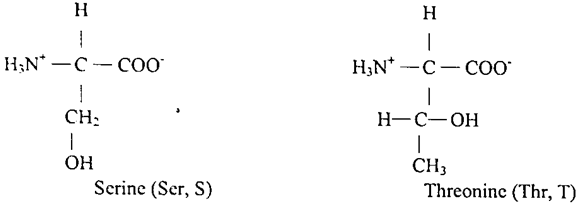

نعاود مرة اخرى جولتنا في الاحماض الامينية ونتكلم عن :

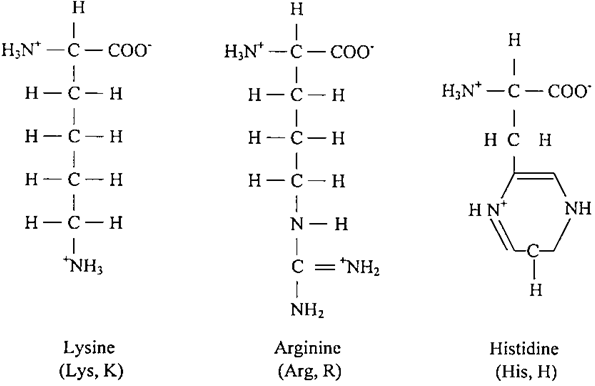
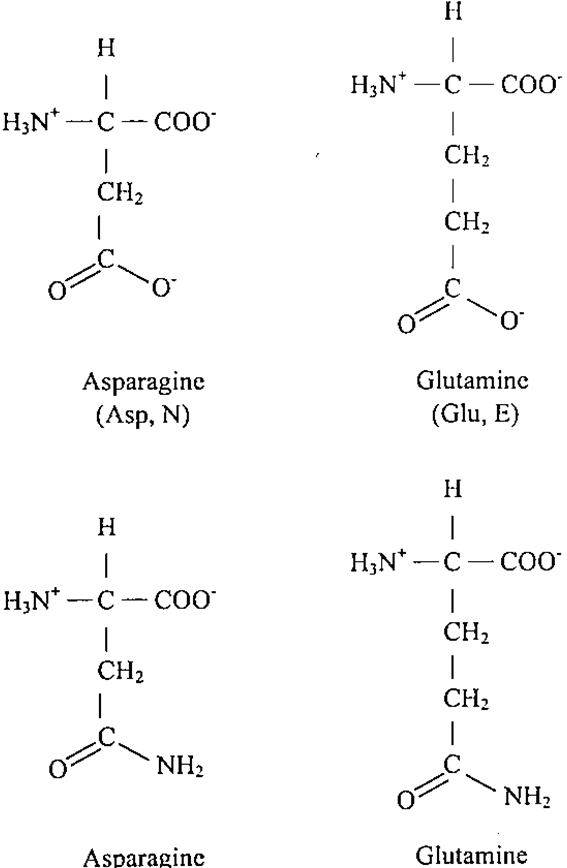

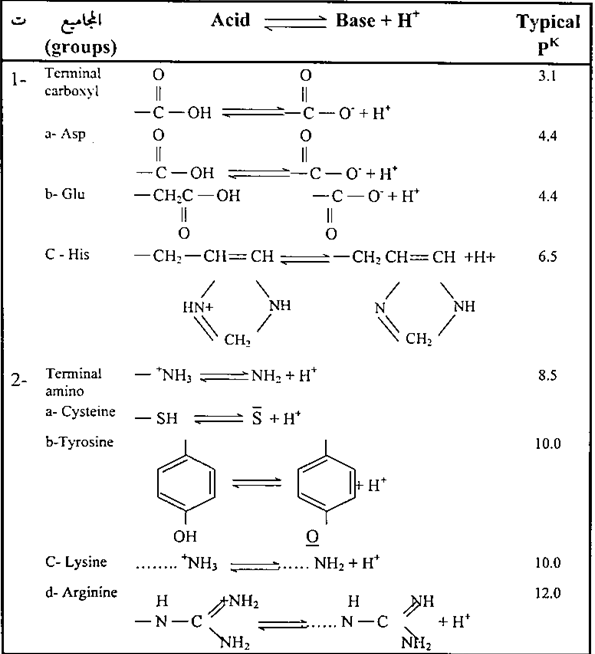
مما سبق نلاحظ ان سبعة أحماض من العشرين حامض أميني لها سلاسل جانبية قابلة للتأين وقد تم توضيح ذلك في قيم التوازن، Pk (ثابت التأين) للسلاسل الجانبية للأرجننين، واللايسين، والهستدين، والإسبارتيك، والكلوتاميك والستين والتايروسين في البروتينات في الجدول التالي :


|
|
|
|
دراسة: إجراء واحد لتقليل المخاطر الجينية للوفاة المبكرة
|
|
|
|
|
|
|
"الملح والماء" يمهدان الطريق لأجهزة كمبيوتر تحاكي الدماغ البشري
|
|
|
|
|
|
بالصور: عند زيارته لمعهد نور الإمام الحسين (عليه السلام) للمكفوفين وضعاف البصر في كربلاء.. ممثل المرجعية العليا يقف على الخدمات المقدمة للطلبة والطالبات
|
|
|
|
ممثل المرجعية العليا يؤكد استعداد العتبة الحسينية لتبني إكمال الدراسة الجامعية لشريحة المكفوفين في العراق
|
|
|
|
ممثل المرجعية العليا يؤكد على ضرورة مواكبة التطورات العالمية واستقطاب الكفاءات العراقية لتقديم أفضل الخدمات للمواطنين
|
|
|
|
العتبة الحسينية تستملك قطعة أرض في العاصمة بغداد لإنشاء مستشفى لعلاج الأورام السرطانية ومركز تخصصي للتوحد
|